- Химики РУДН создали катализатор для получения водорода из воды с помощью света
- В Германии создали вещество для расщепления воды на кислород и водород подобно растениям — Газета.
- Фотокатализатор, способный расщеплять воду на водород и кислород с квантовой эффективностью, близкой к 100% Квантовая эффективность близка к 100%.
- Превратить воду из водорода и кислорода в водородное топливо
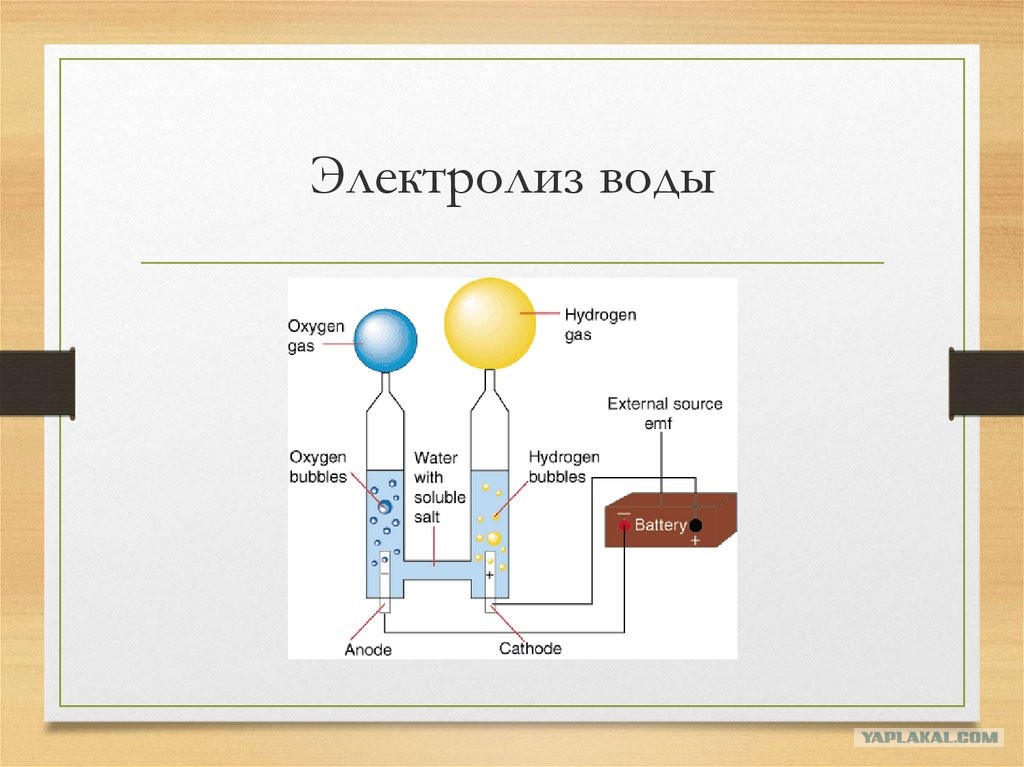
Химики РУДН создали катализатор для получения водорода из воды с помощью света
Химики РУДН вместе с коллегами из Ирана и Финляндии создали трехмерный катализатор для получения водорода из воды при помощи света. Материал состоит из оксида вольфрама на подложке из пористого углерода. Разработка поможет производить водородное топливо решить проблему исчерпаемости нефтепродуктов.
Основной энергетический ресурс современного мира — невозобновляемая нефть. Запасов хватит примерно на 50 лет. Одна из возможных альтернатив — водород. У него высокая энергоемкость, он значительно экологичнее нефти — при его сгорании в окружающую среду выделяется только вода. Но для производства водорода тратится больше энергии, чем потом выделится при сжигании. Химики РУДН совместно с коллегами из Ирана и Финляндии синтезировали трехмерный катализатор, который позволяет получить водород из воды с помощью фотокаталитического разложения, для которого нужен только солнечный свет.
«Синтез трехмерных фотокатализаторов открывает большой потенциал для химических реакций и получения водорода.
Они помогут найти эффективное решение проблем охраны окружающей среды и дефицита энергии», — кандидат наук Хатаии Алиреза, ведущий научный сотрудник факультета физико-математических и естественных наук РУДН.
Фотокаталитическое разложение воды иногда называют искусственным фотосинтезом, потому что оно повторяет одну из стадий этого природного процесса. Чтобы расщепить воду на водород и кислород при помощи света, ее помещают в катализатор. В нем под действием света с определенной длиной волны образуются свободные электроны. Благодаря смещению электронов возникают «дырки» — условные положительные заряды, которые появляются там, где должны были быть электроны. Между электронами и дырками возникает напряжение. Под действием напряжения молекулы воды расщепляются на радикалы — ионы водорода и кислорода. После этого водородный радикал превращается в молекулу H2, а кислородный окисляет содержащиеся в воде органические и неорганические загрязнители. Химики создали катализатор для этого процесса из оксида вольфрама.
Синтез нового материала химики РУДН провели методом самосборки, а в качестве шаблона использовали клетки диатомовых водорослей. На них нанесли каркас из органического соединения, на котором осаждали наночастицы оксида железа. Следом шел слой оксида вольфрама и вспомогательного органического вещества — прекурсора. На следующем этапе ученые нагрели получившийся «бутерброд» так, что прекурсор разложился и превратился в пористую углеродную подложку. Наконец, химики поместили материал в плазменный реактор с атмосферой азота. Это было нужно для внедрения атомов азота в структуру катализатора.
В результате химики РУДН получили пористый материал с большой удельной площадью — в одном грамме умещается около 208 квадратных метров. За один час один килограмм катализатора дает 5,5 граммов водорода. При нормальном давлении это соответствует примерно 61 000 литрам.
Исследование опубликовано в журнале ACS Applied Materials & Interfaces.
В Германии создали вещество для расщепления воды на кислород и водород подобно растениям — Газета.
 Ru
RuВ Германии создали вещество для расщепления воды на кислород и водород подобно растениям — Газета.Ru | Новости
close
100%
Ученые разработали вещество, способное расщеплять молекулы воды на водород и кислород. Статья об этом опубликована в Nature Catalysis.
Работа была проведена Франком Вюртнером из Вюрцбургского университета. Он и его научная группа в течение многих лет работают над искусственным воспроизведением фотосистемы-II, которая в растениях связана с разложением воды в ходе фотосинтеза. Несколько лет назад им удалось создать сложную химическую систему из нескольких различных молекул на базе ионов рутения и органических веществ, которая была способна разлагать молекулы воды.
В ходе этой работы исследователям пришла в голову идея сделать из рутения искусственный фермент для разложения воды. Это было невозможно без нового каталитического центра, способного взять на себя функции сразу нескольких молекул из прошлой работы.
Руководствуясь этой идеей, ученые изучили то, как органические молекулы, окружающие атомы рутения, влияют на характер взаимодействий между водой и центром катализатора. Благодаря этому авторам удалось подобрать требуемую форму трехмерной «оболочки» вокруг ионов рутения, которая заставляла молекулы воды принять оптимальное положение для расщепления.
Впоследствии профессор Вюртнер и его коллеги синтезировали две разных формы этого катализатора, а также детально изучили их структуру и работу на практике. Эти опыты показали, что синтетический фермент действительно способен активно расщеплять воду столь же быстро, как это делает фотосистема-II. В ближайшее время ученые планируют использовать этот фермент для создания экспериментальной установки, расщепляющей воду при помощи энергии света.
Подобная технология может пригодиться для водородной энергетики, поскольку сейчас основную массу водорода извлекают из природного газа.
Ранее геологи спрогнозировали образование единого суперконтинента через 300 млн лет.
Подписывайтесь на «Газету.Ru» в Новостях, Дзен и Telegram.
Чтобы сообщить об ошибке, выделите текст и нажмите Ctrl+Enter
Новости
Дзен
Telegram
Мария Дегтерева
Свой-чужой
О том, как люди сбиваются в стаи в соцсетях
Георгий Бовт
Не виноватые они. Он сам пришел
О том, как демократические институты проложили путь к катастрофе в Германии в 1933-м
Алена Солнцева
Портрет на фоне «Чебурашки»
О национальных российских кинопремиях
Георгий Малинецкий
За клубную работу всерьез!
О функциях РАН
«Дай Откусить»
Еще чашечку
О культуре потребления кофе в России и мире
Найдена ошибка?
Закрыть
Спасибо за ваше сообщение, мы скоро все поправим.
Продолжить чтение
Фотокатализатор, способный расщеплять воду на водород и кислород с квантовой эффективностью, близкой к 100% Квантовая эффективность близка к 100%.
Команда состояла из их коллег из Университета Ямагути, Токийского университета и Национального института передовых промышленных наук и технологий (AIST).
Команда создала идеальную структуру фотокатализатора, состоящую из частиц полупроводника и сокатализаторов. Сокатализаторы выделения h3 и O2 были селективно фотоосаждены на разных гранях кристаллических частиц SrTiO3 (легированных Al) благодаря анизотропному переносу заряда. Эта структура фотокатализатора эффективно предотвращала потери на рекомбинацию зарядов, достигая верхнего предела квантовой эффективности.
Рисунок 1. Схематическая структура (a) и изображение с помощью сканирующего электронного микроскопа (b) легированного алюминием SrTiO3, селективно загруженного сокатализатором выделения водорода (Rh/Cr2O3) и сокатализатором выделения кислорода (CoOOH).
Реакция расщепления воды, управляемая солнечной энергией, представляет собой технологию крупномасштабного производства возобновляемого солнечного водорода. Для практического применения такой технологии необходимо существенно снизить себестоимость производства солнечного водорода [1]. Для этого требуется реакционная система, которая может эффективно расщеплять воду и легко масштабироваться. Система, состоящая из частиц полупроводниковых фотокатализаторов, может быть расширена на большую площадь с помощью относительно простых процессов. Таким образом, будет достигнут большой прогресс в крупномасштабном производстве солнечного водорода, если будут разработаны фотокатализаторы, управляющие реакцией расщепления воды под действием солнечного света с высокой эффективностью.
Чтобы повысить эффективность преобразования солнечной энергии при фотокаталитическом расщеплении воды, необходимо улучшить два фактора: расширить диапазон длин волн света, используемого фотокатализатором для реакции, и увеличить квантовый выход на каждой длине волны. Первое определяется шириной запрещенной зоны используемого фотокаталитического материала, а второе определяется качеством фотокаталитического материала и функциональностью сокатализатора, используемого для ускорения реакции. Однако фотокаталитическое расщепление воды является эндергонической реакцией с многоэлектронным переносом, происходящей в неравновесном состоянии.
В этом исследовании были усовершенствованы конструкция и принцип работы усовершенствованных методов расщепления воды с высокой квантовой эффективностью. Знания, полученные в этом исследовании, будут способствовать дальнейшему развитию области фотокаталитического расщепления воды, чтобы обеспечить масштабируемое производство солнечного водорода.
Проект стал возможен благодаря поддержке NEDO (Организация по развитию новых энергетических и промышленных технологий) в рамках «Проекта искусственного фотосинтеза».
Название: Фотокаталитическое расщепление воды с квантовой эффективностью, близкой к единице
Авторы: Цуёси Таката, Цзюньчжэ Цзян, Ёсихиса Саката, Мамико Накабаяси, Наоя Шибата, Викас Нандал, Казухико Секи, Такаси Хисатоми, Казунари Домен -2278-9
Превратить воду из водорода и кислорода в водородное топливо
22.03.2022
устойчивость
В Корее родственники дарят жениху и невесте деревянных уточек. Почему? Потому что считается, что эти водоплавающие птицы образуют особенно прочные связи. Деревянные уточки символизируют свадьбу молодоженов.
Такие элементы, как водород и кислород, также вступают в тесные связи — они соединяются вместе, образуя воду, и требуется много усилий и энергии, чтобы их разделить. Сам по себе водород чрезвычайно летуч. Обычно он бесцветный и безвкусный. Молекула его газа состоит из двух атомов, которые можно хранить под высоким давлением — предпочтительно в тщательно запечатанных резервуарах или газовых баллонах. На самом деле водород не хочет ничего, кроме воссоединения с кислородом, чтобы снова стать жидкой водой. В процессе водород высвобождает часть энергии, затраченной во время разделения — эффект, который можно использовать для производства и потребления энергии в климатически нейтральном цикле.
Сам по себе водород чрезвычайно летуч. Обычно он бесцветный и безвкусный. Молекула его газа состоит из двух атомов, которые можно хранить под высоким давлением — предпочтительно в тщательно запечатанных резервуарах или газовых баллонах. На самом деле водород не хочет ничего, кроме воссоединения с кислородом, чтобы снова стать жидкой водой. В процессе водород высвобождает часть энергии, затраченной во время разделения — эффект, который можно использовать для производства и потребления энергии в климатически нейтральном цикле.
Вы можете найти PDF-файл с полной инфографикой здесь.
СТАНЦИЯ 1 |
ОСНОВЫ ВОДЫ
Как уже упоминалось, вода состоит из водорода и кислорода. Один атом кислорода и два атома водорода образуют молекулу воды. В природе вода обычно содержит растворенные газы, органические соединения и соли. В целом 71 процент земной поверхности покрыт водой. Общий объем воды составляет 1,4 миллиарда кубических километров, 3,5 процента из которых составляют пресные воды. Это соответствует 48 миллионам кубических километров. Если бы это количество воды было сжато в куб, длина его граней составила бы целых 363 километра. Итак, вода существует на планете в огромном количестве, но распределена она неравномерно.
Это соответствует 48 миллионам кубических километров. Если бы это количество воды было сжато в куб, длина его граней составила бы целых 363 километра. Итак, вода существует на планете в огромном количестве, но распределена она неравномерно.
СТАНЦИЯ 2 |
КЛИМАТИЧЕСКИ НЕЙТРАЛЬНАЯ ГЕНЕРАЦИЯ ЭЛЕКТРОЭНЕРГИИ
Электричество можно производить с помощью гидроэнергетики или с помощью энергии солнца и ветра. Компании и потребители получают электроэнергию, выработанную этими способами. При благоприятных погодных условиях – например, в солнечные периоды или ветреные осенние дни – можно произвести больше электроэнергии, чем необходимо. Воздействие может быть увеличено за счет расширения объектов возобновляемой энергии в стране. Излишки электроэнергии могут быть либо использованы сразу, либо сохранены. И здесь на помощь приходит водород. Излишки электроэнергии можно использовать для производства водорода путем электролиза на специальных установках.
СТАНЦИЯ 3 |
УСТАНОВКА ДЛЯ ЭЛЕКТРОЛИЗА
Что именно происходит в системе электролиза? Электричество применяется к воде внутри него. Энергия разделяет воду на кислород и водород. Как правило, для этого используется пресная вода. Но исследователи уже работают над каталитическими нейтрализаторами, которые могли бы использовать морскую воду для электролиза водорода. Сегодня установленные предприятия обращаются к процессу с использованием мембраны, проницаемой только для протонов. Мембрана действует как сепаратор, расположенный между катодом и анодом. По сути топливный элемент, только наоборот. Если подается внешнее напряжение, это вызывает разложение воды на аноде. В результате образуются ионы водорода, свободные электроны и кислород. Только ионы водорода проходят через мембрану и достигают катода. Там они соединяются со свободными электронами, образуя водород.
СТАНЦИЯ 4 |
ПЕРЕВОЗКА ВОДОРОДА
Транспортные средства, приводимые в движение топливными элементами, могут работать на водороде.
СТАНЦИЯ 5 |
СТАНЦИЯ ЗАПРАВКИ ВОДОРОДОМ
Процессы заправки водородом мало что меняют для современных владельцев транспортных средств, хотя насосы работают немного иначе, чем обычные ТРК. Следует отметить, что бак в легковом или грузовом автомобиле на топливных элементах необходимо заправлять под высоким давлением. Водород поступает из блока подачи в автомобиль под давлением около 700 бар. Топливный шланг должен быть плотно закреплен на муфте, прикрепленной к штуцеру бака на автомобиле. Затем топливный шланг автоматически затягивается. Инфракрасный интерфейс принимает данные о транспортном средстве, важные для процесса заправки, и передает их насосу. Чтобы заполнить бак автомобиля, требуется до четырех минут — чуть дольше, чем сопоставимая заправка бензином или дизельным топливом. А вот запас хода у автомобилей на водороде чуть меньше: от 400 до 500 километров.
Водород поступает из блока подачи в автомобиль под давлением около 700 бар. Топливный шланг должен быть плотно закреплен на муфте, прикрепленной к штуцеру бака на автомобиле. Затем топливный шланг автоматически затягивается. Инфракрасный интерфейс принимает данные о транспортном средстве, важные для процесса заправки, и передает их насосу. Чтобы заполнить бак автомобиля, требуется до четырех минут — чуть дольше, чем сопоставимая заправка бензином или дизельным топливом. А вот запас хода у автомобилей на водороде чуть меньше: от 400 до 500 километров.
СТАНЦИЯ 6 |
ТРАНСПОРТНЫЕ СРЕДСТВА НА ТОПЛИВНЫХ ЭЛЕМЕНТАХ
Даже если процесс заправки похож на заправку двигателя внутреннего сгорания, водород приводит в действие электромобиль. Его топливный элемент преобразует водород в электроэнергию, питающую электродвигатель. По отношению к своей массе водород имеет огромную плотность энергии. Преимущество: использование водорода позволяет грузовикам и автобусам преодолевать большие расстояния, которые им необходимы. Но есть и большой недостаток: водород очень легкий. По отношению к объему его плотность энергии довольно низка. Это приводит к необходимости его значительного сжатия. Даже в этом случае баки занимают больше места, чем обычные топливные баки. С другой стороны, им требуется значительно меньше места, чем сегодняшним ионно-литиевым батареям.
Но есть и большой недостаток: водород очень легкий. По отношению к объему его плотность энергии довольно низка. Это приводит к необходимости его значительного сжатия. Даже в этом случае баки занимают больше места, чем обычные топливные баки. С другой стороны, им требуется значительно меньше места, чем сегодняшним ионно-литиевым батареям.
СТАНЦИЯ 7 |
ТОПЛИВНЫЙ ЭЛЕМЕНТ
Так работают топливные элементы: положительно заряженные ионы водорода мигрируют в нем от анода к катоду. На своем пути они проходят через мембрану из полимерного электролита. Там они реагируют с кислородом воздуха, оставляя после себя воду. Во время этого процесса на аноде образуется избыток отрицательно заряженных электронов водорода. Если вы соедините эти электроны водорода с катодом через отдельную силовую цепь, они будут мигрировать туда. Это означает, что протекает электрический ток, но он составляет всего около 50 процентов от тока, который первоначально использовался для производства водорода.