- собираем действующую установку своими руками. Электролизер водорода своими руками
- Принцип работы и преимущества генератора водорода: функциональные особенности
- Перекись водорода как устойчивый носитель энергии: электрокаталитическое производство перекиси водорода и топливный элемент
- Microsoft тестирует генераторы водорода — топливные элементы Microsoft
собираем действующую установку своими руками. Электролизер водорода своими руками
Содержание
Устройство и принцип работы генератора водорода
Заводской генератор водорода представляет собой внушительный агрегат
Использовать водород в качестве топлива для обогрева загородного дома выгодно не только по причине высокой теплотворной способности, но и потому, что в процессе его сжигания не выделяется вредных веществ. Как все помнят из школьного курса химии, при окислении двух атомов водорода (химическая формула h3 – Hidrogenium) одним атомом кислорода, образуется молекула воды. При этом выделяется в три раза больше тепла, чем при сгорании природного газа. Можно сказать, что равных водороду среди других источников энергии нет, поскольку его запасы на Земле неисчерпаемы — мировой океан на 2/3 состоит из химического элемента h3, да и во всей Вселенной этот газ наряду с гелием является главным «строительным материалом». Вот только одна проблема — для получения чистого h3 надо расщепить воду на составляющие части, а сделать это непросто. Учёные долгие годы искали способ извлечения водорода и остановились на электролизе.
Учёные долгие годы искали способ извлечения водорода и остановились на электролизе.
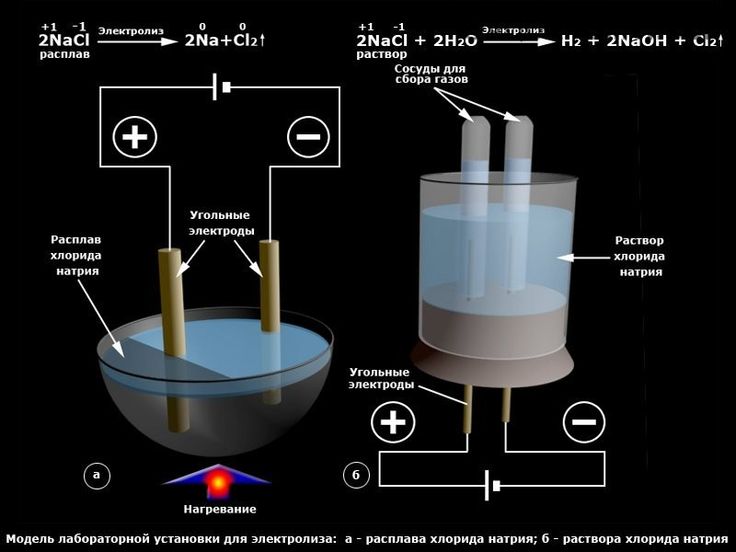
Схема работы лабораторного электролизёра
Этот способ получения летучего газа заключается в том, что в воду на небольшом расстоянии друг от друга помещаются две металлические пластины, подключённые к источнику высокого напряжения. При подаче питания высокий электрический потенциал буквально разрывает молекулу воды на составляющие, высвобождая два атома водорода (HH) и один — кислорода (O). Выделяющийся газ назвали в честь физика Ю. Брауна. Его формула — HHO, а теплотворная способность — 121 МДж/кг. Газ Брауна горит открытым пламенем и не образует никаких вредных веществ. Главное достоинство этого вещества в том, что для его использования подойдёт обычный котёл, работающий на пропане или метане. Заметим только, что водород в соединении с кислородом образует гремучую смесь, поэтому потребуются дополнительные меры предосторожности.
Схема установки для получения газа Брауна
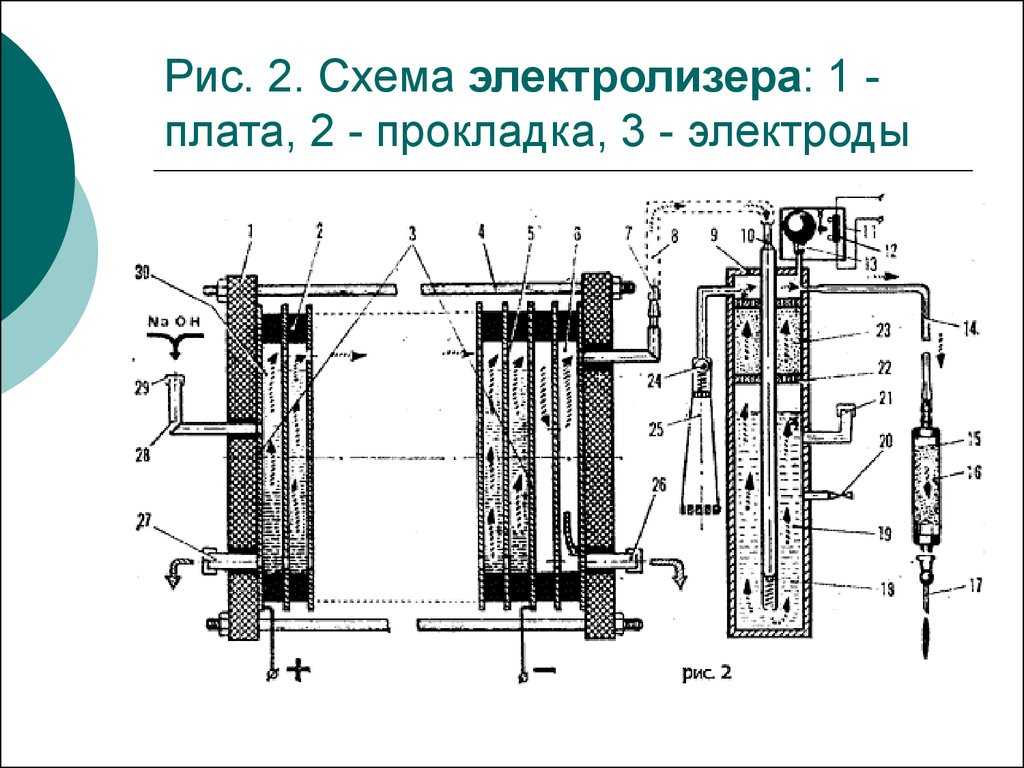
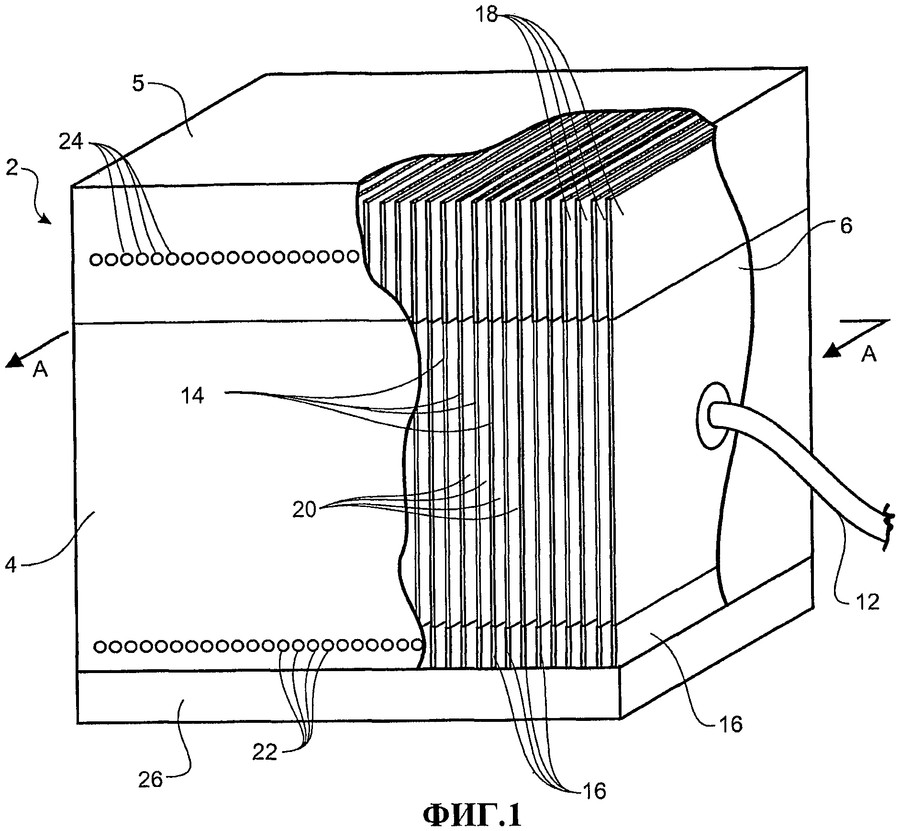
Генератор, предназначенный для получения газа Брауна в больших количествах, содержит несколько ячеек, каждая из которых вмещает в себя множество пар пластин-электродов.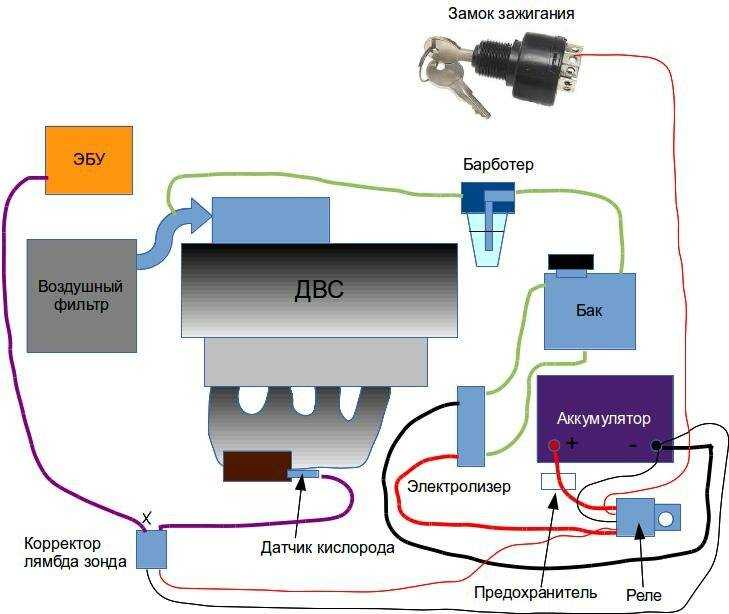 Они установлены в герметичной ёмкости, которая оборудована выходным патрубком для газа, клеммами для подключения питания и горловиной для заливки воды. Кроме того, установка оборудуется защитным клапаном и водяным затвором. Благодаря им устраняется возможность распространения обратного пламени. Водород горит только на выходе из горелки, а не воспламеняется во все стороны. Многократное увеличение полезной площади установки позволяет извлекать горючее вещество в количествах, достаточных для различных целей, включая обогрев жилых помещений. Вот только делать это, используя традиционный электролизёр, будет нерентабельно. Проще говоря, если потраченное на добычу водорода электричество напрямую использовать для отопления дома, то это будет намного выгоднее, чем топить котёл водородом.
Они установлены в герметичной ёмкости, которая оборудована выходным патрубком для газа, клеммами для подключения питания и горловиной для заливки воды. Кроме того, установка оборудуется защитным клапаном и водяным затвором. Благодаря им устраняется возможность распространения обратного пламени. Водород горит только на выходе из горелки, а не воспламеняется во все стороны. Многократное увеличение полезной площади установки позволяет извлекать горючее вещество в количествах, достаточных для различных целей, включая обогрев жилых помещений. Вот только делать это, используя традиционный электролизёр, будет нерентабельно. Проще говоря, если потраченное на добычу водорода электричество напрямую использовать для отопления дома, то это будет намного выгоднее, чем топить котёл водородом.
Водородная топливная ячейка Стенли Мейера
Выход из сложившейся ситуации нашёл американский учёный Стенли Мейер. Его установка использовала не мощный электрический потенциал, а токи определённой частоты. Изобретение великого физика состояло в том, что молекула воды раскачивалась в такт изменяющимся электрическим импульсам и входила в резонанс, который достигал силы, достаточной для её расщепления на составляющие атомы. Для такого воздействия требовались в десятки раз меньшие токи, чем при работе привычной электролизной машины.
Изобретение великого физика состояло в том, что молекула воды раскачивалась в такт изменяющимся электрическим импульсам и входила в резонанс, который достигал силы, достаточной для её расщепления на составляющие атомы. Для такого воздействия требовались в десятки раз меньшие токи, чем при работе привычной электролизной машины.
Видео: Топливная ячейка Стенли Мейера
За своё изобретение, которое могло бы освободить человечество от кабалы нефтяных магнатов, Стенли Мейер был убит, а труды его многолетних изысканий пропали неизвестно куда. Тем не менее сохранились отдельные записи учёного, на основании которых изобретатели многих стран мира пытаются строить подобные установки. И надо сказать, небезуспешно.
Преимущества газа Брауна как источника энергии
- Вода, из которой получают HHO, является одним из наиболее распространённых веществ на нашей планете.

- При сгорании этого вида топлива образуется водяной пар, который можно обратно конденсировать в жидкость и повторно использовать в качестве сырья.
- В процессе сжигания гремучего газа не образуется никаких побочных продуктов, кроме воды. Можно сказать, что нет более экологичного вида топлива, чем газ Брауна.
- При эксплуатации водородной отопительной установки выделяется водяной пар в количестве, достаточном для поддержания влажности в помещении на комфортном уровне.
Вам также может быть интересен материал о том, как соорудить самостоятельно газовый генератор: https://aqua-rmnt.com/otoplenie/kotly/gazogenerator-na-drovakh-dlya-otopleniya-doma-svoimi-rukami.html
Область применения
Сегодня электролизёр — такое же привычное устройство, как и генератор ацетилена или плазменный резак. Изначально водородные генераторы использовались сварщиками, поскольку носить за собой установку весом всего несколько килограмм было намного проще, чем перемещать огромные кислородные и ацетиленовые баллоны. При этом высокая энергоёмкость агрегатов решающего значения не имела — всё определяло удобство и практичность. В последние годы применение газа Брауна вышло за рамки привычных понятий о водороде, как топливе для газосварочных аппаратов. В перспективе возможности технологии очень широки, поскольку использование HHO имеет массу достоинств.
При этом высокая энергоёмкость агрегатов решающего значения не имела — всё определяло удобство и практичность. В последние годы применение газа Брауна вышло за рамки привычных понятий о водороде, как топливе для газосварочных аппаратов. В перспективе возможности технологии очень широки, поскольку использование HHO имеет массу достоинств.
- Сокращение расхода горючего на автотранспорте. Существующие автомобильные генераторы водорода позволяют использовать HHO как добавку к традиционному бензину, дизелю или газу. За счёт более полного сгорания топливной смеси можно добиться 20 – 25 % снижения потребления углеводородов.
- Экономия топлива на тепловых электростанциях, использующих газ, уголь или мазут.
- Снижение токсичности и повышение эффективности старых котельных.
- Многократное снижение стоимости отопления жилых домов за счёт полной или частичной замены традиционных видов топлива газом Брауна.
- Использование портативных установок получения HHO для бытовых нужд — приготовления пищи, получения тёплой воды и т.
 д.
д. - Разработка принципиально новых, мощных и экологичных силовых установок.
Генератор водорода, построенный с использованием «Технологии водяных топливных ячеек» С. Мейера (а именно так назывался его трактат) можно купить — их изготовлением занимается множество компаний в США, Китае, Болгарии и других странах. Мы же предлагаем изготовить водородный генератор самостоятельно.
Видео: Как правильно обустроить водородное отопление
Типы установок
На сегодняшний день водородный генератор для автомобиля может быть укомплектован тремя различными по типу, характеру работы и производительности электролизёрами:
- Простой, цилиндрического типа. Производит 700 миллилитров газа в минуту. Такой производительности достаточно для двигателей с рабочим объёмом до 1,4 литров.
- С ячейками раздельного типа. Является самым эффективным по типу конструкции и производительности. Выход газа превышает 2 литра в минуту. Такой объём позволяет применять его на грузовом транспорте.
- Электролизёр с пластинами открытого типа. Эта конструкция обеспечивает дополнительное охлаждение системе, в результате чего может использоваться при длительной работе агрегата. Выход газа регулируется количеством пластин реактора.
Первый тип конструкции вполне достаточен для множества карбюраторных двигателей. Отсутствует необходимость в установке сложной электронной схемы регулятора производительности газа, да и сама сборка такого электролизёра не представляет сложности.
Для более мощных автомобилей предпочтительна сборка второго типа реактора. А для двигателей, работающих на дизельном топливе, и большегрузных машин используют третий тип реактора.
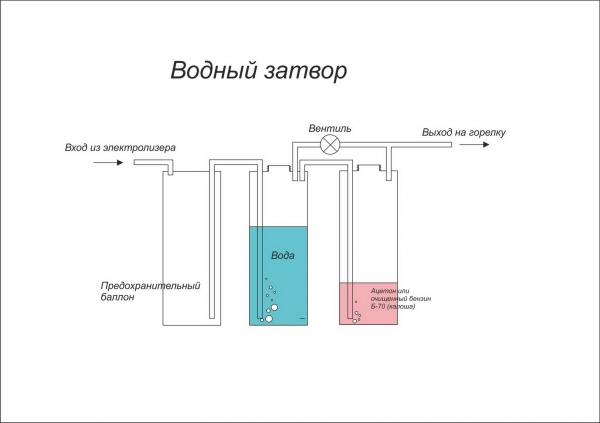
Делаем простейший генератор водорода своими руками пошагово
Расскажем, как можно сделать самодельный генератор для получения смеси водорода и кислорода (ННО). Его мощности на отопления дома не хватит, но для газовой горелки для резки металла количество полученного газа будет достаточным.
Его мощности на отопления дома не хватит, но для газовой горелки для резки металла количество полученного газа будет достаточным.
Обозначения:
- а – сопло горелки;
- b – трубки;
- c – водные затворы;
- d – вода;
- е – электроды;
- f – герметичный корпус.
В первую очередь делаем электролизер, для этого нам понадобится герметичная емкость и электроды. В качестве последних используем стальные пластины (их размер выбираем произвольно, в зависимости от желаемой производительности), прикрепленные к диэлектрическому основанию. Соединяем между собой все пластины каждого из электродов.
Когда электроды готовы их надо укрепить в емкости таким образом, чтобы места подключения проводов питания были выше предполагаемого уровня воды. Провода от электродов идут к блоку питания на 12 вольт или автомобильному аккумулятору.
В крышке емкости делаем отверстие под трубку для выхода газа. В качестве водных затворов можно использовать обычные стеклянные банки емкостью 1 литр.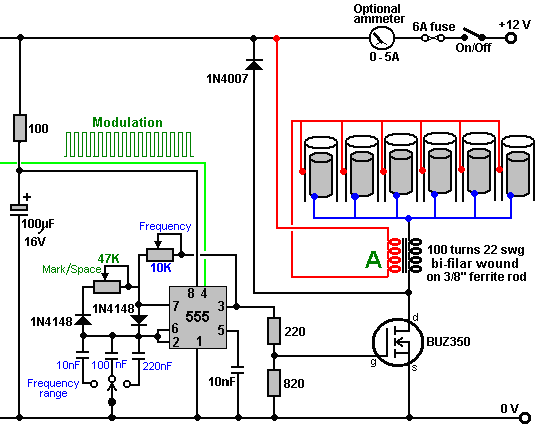 Заполняем их на 2/3 водой и подключаем к электролизеру и горелке, как показано на рисунке 8.
Заполняем их на 2/3 водой и подключаем к электролизеру и горелке, как показано на рисунке 8.
Горелку лучше взять готовую, поскольку не каждый материал может выдержать температуру горения газа Брауна. Подключаем ее к выходу последнего водного затвора.
Наполняем электролизер водой, в которую добавлена обычная кухонная соль.
Подаем напряжение на электроды и проверяем работу устройства.
Давно уже прошли те времена, когда загородный дом можно было обогреть лишь одним способом — сжигая в печке дрова или уголь. Современные отопительные приборы используют различные виды топлива и при этом автоматически поддерживают комфортную температуру в наших жилищах. Природный газ, дизель или мазут, электричество, гелио- и геотермальное тепло — вот неполный список альтернативных вариантов. Казалось бы — живи и радуйся, да вот только постоянный рост цен на топливо и оборудование вынуждает продолжать поиски дешёвых способов отопления. А вместе с тем неиссякаемый источник энергии — водород, буквально лежит у нас под ногами. И сегодня мы поговорим о том, как использовать в качестве горючего обычную воду, собрав генератор водорода своими руками.
И сегодня мы поговорим о том, как использовать в качестве горючего обычную воду, собрав генератор водорода своими руками.
Электролизер для автомобиля своими руками
В интернете можно найти много схем HHO систем, которые, если верить авторам, позволяют экономить от 30% до 50% топлива. Такие заявления слишком оптимистичны и, как правило, не подтверждаются никакими доказательствами. Упрощенная схема такой системы продемонстрирована на 11 рисунке.
Упрощенная схема электролизера для автомобиля
По идее, такое устройство должно снизить расход топлива за счет его полного выгорания. Для этого в воздушный фильтр топливной системы подается смесь Брауна. Это водород с кислородом, полученные из электролизера, запитанного от внутренней сети автомобиля, что повышает расход топлива. Замкнутый круг.
Безусловно, может быть задействована схема шим регулятора силы тока, использован более эффективный импульсный блок питания или другие хитрости, позволяющие снизить расход энергии. Иногда в интернете попадаются предложения приобрести низкоамперный БП для электролизера, что вообще является нонсенсом, поскольку производительность процесса напрямую зависит от силы тока.
Иногда в интернете попадаются предложения приобрести низкоамперный БП для электролизера, что вообще является нонсенсом, поскольку производительность процесса напрямую зависит от силы тока.
Это как система Кузнецова, активатор воды которой утерян, а патент отсутствует и т.д. В приведенных видео, где рассказывают о неоспоримых преимуществах таких систем, практически нет аргументированных доводов. Это не значит, что идея не имеет прав на существование, но заявленная экономия «слегка» преувеличена.
Опасность водородного топлива
В рассмотренных выше недостатках упоминалось об опасности применения водородного топлива для двигателя. Это главный минус новой технологии.
В сочетании с окислителем (кислородом) возрастает риск воспламенения водорода или даже взрыва. Проведенные исследования показали, что для воспламенения h3 достаточно 1/10 части энергии, необходимой для зажигания бензиновой смеси. Другими словами, для вспыхивания водорода хватит и статической искры.
Еще одна опасность заключается в невидимости водородного пламени. При горении вещества огонь почти незаметен, что усложняет процесс борьбы с ним. Кроме того, чрезмерное количество h3 приводит к появлению удушья.
При горении вещества огонь почти незаметен, что усложняет процесс борьбы с ним. Кроме того, чрезмерное количество h3 приводит к появлению удушья.
Опасность в том, что распознать данный газ крайне сложно, ведь у него нет запаха и он полностью невидим для человеческого глаза.
Кроме того, сжиженный h3 имеет низкую температуру, поэтому в случае утечки с открытыми частями тела высок риск серьезного обморожения. Находится данный газ должен в специальных хранилищах.
Принцип работы и преимущества генератора водорода: функциональные особенности
По ряду объективных причин водород практически не встречается на Земле в свободном виде. При этом водород необходим для решения множества производственных задач, он используется в лабораторных исследованиях, пищевой и химической промышленности. Чтобы получить чистый газ приходится работать с соединениями, в которых присутствуют молекулы водорода, задействовав соответствующую химическую реакцию. Наиболее распространенные методики выделения водоворота в промышленности:
Чтобы получить чистый газ приходится работать с соединениями, в которых присутствуют молекулы водорода, задействовав соответствующую химическую реакцию. Наиболее распространенные методики выделения водоворота в промышленности:
- высокотемпературная обработка метана;
- реакция разложения сероводорода;
- взаимодействие концентрированных кислот и металлов;
- реакция разложения гидрида натрия;
- электролитическое разложение воды.
Выбор способа выработки водорода обусловлен техническими условиями производства. При этом наиболее универсальным методом считается электролиз дистиллированной воды.
Далее будет описана схема, как работает генератор водорода и какие преимуществами он обладает.
Функциональные особенности электролитических генераторов
Сырьем для продуцирования водорода выступает дистиллят глубокой очистки. Поскольку даже небольшое количество примесей, растворенных в воде, влияют на качество и чистоту готового продукта, на предварительном этапе вода пропускается через деионизационный фильтр. Дальнейшая последовательность выделения водорода состоит из следующих этапов:
Дальнейшая последовательность выделения водорода состоит из следующих этапов:
- Дистиллят поступает в электролизер — устройство, в котором совершается расщепления молекул воды под воздействием электрического тока. Так как дистиллированная вода, лишенная солей, не является токопроводящей средой, задачу электролита выполнят ионообменная мембрана.
- Образовавшийся кислород выводится из системы и может быть использован в работе при решении других производственных задач;
- Водород осушается от влаги и проходит через дополнительную очистку от остаточного молекулярного кислорода.
Набор и производительность оборудования, входящего в состав генерирующего комплекса, подбирается индивидуально, в зависимости от технологических требований производства. Опционально установка может комплектоваться системой охлаждения, агрегатом для предварительной подготовки воды и другими модулями.
Наша продукция
Смотреть каталог
Какими преимуществами обладают генераторы водорода
Если сравнивать с традиционным способом подачи водорода посредством сменных баллонов, применение генераторных установок обладает рядом существенных преимуществ.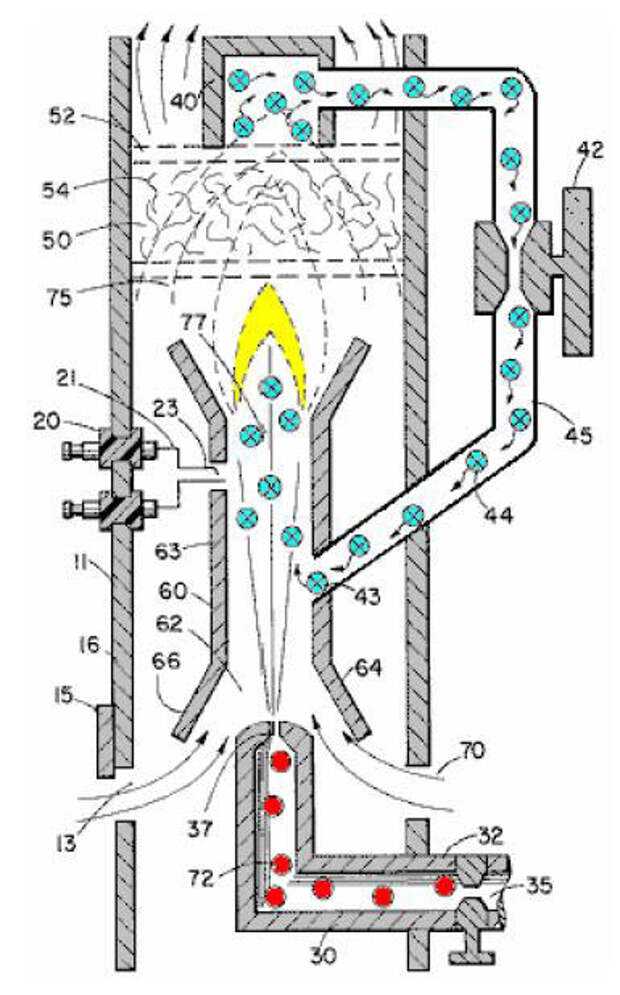 Прежде всего речь идет о снижении затрат на доставку и хранение запасов водорода. Также следует упомянуть о таких особенностях:
Прежде всего речь идет о снижении затрат на доставку и хранение запасов водорода. Также следует упомянуть о таких особенностях:
- Полученный электролизом водород после просушивания и фильтрации обладает степенью очистки в пределах 99,9998%, позволяющей использовать газ для любых производственных и научных задач.
- Процесс выработки газа автоматизирован. Рабочие режимы системы поддаются тонкой настройке, а качество полученного водорода постоянно контролируется оператором.
- Водород производится в требуемых объемах, отсутствует необходимость в хранении излишков.
- Риск создания пожароопасной ситуации сведен к минимуму.
Производительность генератора, в зависимости от модели электролизера, может варьироваться в пределах 2,8–3500 Нм3/час, а исходящее давление готового водорода: 6–10 БАР. Данные параметры соответствуют требованиям большинства технологических процессов, а значит в при внедрении генератора в производственную линию предварительная адаптация и перенастройка оборудования не потребуются.
Читайте также
Использование азота и кислорода в стекольной промышленности
Продажа оборудования для насыщения воды кислородом
Лабораторный генератор водорода
Чистота азота для лазерной резки
У вас остались вопросы?
Оставьте заявку на бесплатную консультацию у наших менеджеров!
Нажимая кнопку, Вы даете согласие на обработку персональных данных.
География поставок
ООО «Петрошина» г. Санкт-Петербург
Концентрация газа, %: 99,9
Производительность по азоту, Нм3/час: 40
Точка росы азота: — 70
Подробнее
Новости
19 сентября 2019
Участие в 18-й международной специализированной выставке «International Specialized Exhibition»
09 января 2019
Азотная станция для производства лакокрасочной продукции
29 декабря 2018
С наступающим Новым Годом и Рождеством!
22 ноября 2018
Поставлена станция по производству Биогона
01 ноября 2018
Участие в 17-й международной специализированной выставке «International Specialized Exhibition»
29 октября 2018
Приглашаем на выставку Криоген-Экспо. Промышленные газы — 2018
Промышленные газы — 2018
04 октября 2018
Участие в 12-й международной специализированной выставке «ТЕРМООБРАБОТКА»
02 октября 2018
Участие в выставке «Термообработка»
04 июля 2018
Азотная станция для лазерной резки
10 апреля 2018
Металлурги выбирают «Оксимат»Перекись водорода как устойчивый носитель энергии: электрокаталитическое производство перекиси водорода и топливный элемент
1. Seinfeld JH. Айше Дж. 2011; 57:3259. [Google Scholar]
2. Ройер Д.Л., Бернер Р.А., Парк Дж. Природа. 2007; 446:530. [PubMed] [Google Scholar]
3. Льюис Н.С., Носера Д.Г. Proc Natl Acad Sci USA. 2006;103:15729. [Бесплатная статья PMC] [PubMed] [Google Scholar]
4. Nocera DG. Chem Soc Rev. 2009; 38:13. [PubMed] [Google Scholar]
5. Грей HB. Нац. хим. 2009 г.;1:7. [PubMed] [Google Scholar]
6. Jiao F, Frei H. Energy Environ Sci. 2010;3:1018. [Google Scholar]
Jiao F, Frei H. Energy Environ Sci. 2010;3:1018. [Google Scholar]
7. Balzani V, Credi A, Venturi M. ChemSusChem. 2008; 1:26. [PubMed] [Google Scholar]
8. Fukuzumi S. Eur J Inorg Chem. 2008:1351. [Google Scholar]
9. Дау Х., Захариева И. Acc Chem Res. 2009; 42:1861. [PubMed] [Google Scholar]
10. Гаст Д., Мур Т.А., Мур А.Л. Acc Chem Res. 2009;42:1890. [PubMed] [Google Scholar]
11. Fukuzumi S, Yamada Y, Suenobu T, Ohkubo K, Kotani H. Energy Environ Sci. 2011;4:2754. [Академия Google]
12. Момирлан М., Везироглуб Т.Н. Международная водородная энергия. 2005;30:795. [Google Scholar]
13. Данн С. Энциклопедия энергетики. Том. 3. Эльзевир Инк; 2004. с. 241. [Google Scholar]
14. Fukuzumi S, Kobayashi T, Suenobu T. ChemSusChem. 2008; 1:827. [PubMed] [Google Scholar]
15. Baldi A, Dam B. J Mater Chem. 2011;21:4021. [Google Scholar]
16. Шлапбах Л., Цюттель А. Природа. 2001; 414:353. [PubMed] [Google Scholar]
17. Rowsell JLC, Yaghi OM. Angew Chem Int Ed. 2005;44:4670. [PubMed] [Академия Google]
Rowsell JLC, Yaghi OM. Angew Chem Int Ed. 2005;44:4670. [PubMed] [Академия Google]
18. Блюм М.Э., Брэдли М.Г., Баттерик Р., III, Кусари У., Снеддон Л.Г. J Am Chem Soc. 2006; 128:7748. [PubMed] [Google Scholar]
19. Оринакова Р., Оринак А. Топливо. 2011;90:3123. [Google Scholar]
20. Yamanaka I, Murayama T. Angew Chem Int Ed. 2008;47:1900. [PubMed] [Google Scholar]
21. Дисселькамп Р.С. Международная водородная энергия. 2010;35:1049. [Google Scholar]
22. Дисселькамп Р.С. Энергетическое топливо. 2008; 22:277. [Google Scholar]
23. Санли А.Е., Айтак А. Int J Hydrogen Energy. 2011;36:869. [Google Scholar]
24. Yamada Y, Fukunishi Y, Yamazaki S, Fukuzumi S. Chem Commun. 2010;46:7334. [PubMed] [Google Scholar]
25. Nishimi T, Kamachi T, Kato K, Kato T, Yoshizawa K. Eur J Org Chem. 2011:4113. [Google Scholar]
26. Fukuzumi S, Ishikawa K, Tanaka T. Chem Lett. 1986:1. [Google Scholar]
27. Fukuzumi S, Chiba M, Ishikawa M, Ishikawa K, Tanaka T. J Chem Soc, Perkin Trans. 1989; 2:1417. [Google Scholar]
J Chem Soc, Perkin Trans. 1989; 2:1417. [Google Scholar]
28. Sawyer DT, Calderwood TS, Yamaguchi K, Angelis CT. Неорг хим. 1983;22:2577. [Google Scholar]
29. Sargeson AM, Lay PA. Aust J Chem. 2009;62:1280. [Google Scholar]
30. Creaser II, Geue RJ, Mac J, Harrowfield B, Herlt AJ, Sargeson AM, Snow MR, Springborg J. J Am Chem Soc. 1982;104:6016. [Google Scholar]
31. Fukuzumi S, Mochizuki S, Tanaka T. Inorg Chem. 1989; 28:2459. [Google Scholar]
32. Fukuzumi S, Okamoto K, Gros CP, Guilard R. J Am Chem Soc. 2004; 126:10441. [PubMed] [Google Scholar]
33. Маркус Р.А. Ann Rev Phys Chem. 1964;15:155. [Google Scholar]
34. Ян Э.С., Чан М.С., Валь А.С. J Phys Chem. 1988;84:3094. [Google Scholar]
35. Рорбах Д.Ф., Дойч Э., Хайнеман В.Р., Пастернак Р.Ф. Неорг хим. 1977;16:2650. [Google Scholar]
36. Пастернак Р.Ф., Спиро Э.Г. J Am Chem Soc. 1978;100:968. [Google Scholar]
37. Langley R, Hambright P. Inorg Chem. 1985; 24:1267. [Google Scholar]
[Google Scholar]
38. Collman JP, Hutchison JE, Lopez MA, Tabard A, Guilard R, Seok WK, Ibers JA, L’Her M. J Am Chem Soc. 1992;114:9869. [Google Scholar]
39. Bolze F, Gros CP, Drouin M, Espinosa E, Harvey PD, Guilard R. J Organomet Chem. 2002; 643–644:89. [Google Scholar]
40. Chang CJ, Deng Y, Shi C, Chang CK, Anson FC, Nocera DG. хим. коммун. 2000:1355. [Google Scholar]
41. Chang CJ, Baker EA, Pistorio BJ, Deng Y, Loh Z-H, Miller SE, Carpenter SD, Nocera DG. Неорг хим. 2002;41:3102. [PubMed] [Google Scholar]
42. Schmidt S, Heinemann FW, Grohmann A. Eur J Inorg Chem. 2000:1657. [Академия Google]
43. Дай X, Капур П., Уоррен Т.Х. J Am Chem Soc. 2004; 126:4798. [PubMed] [Google Scholar]
44. Hikichi S, Yoshizawa M, Sasakura Y, Komatsuzaki H, Moro-oka Y, Akita M. Chem Eur J. 2001;7:5011. [PubMed] [Google Scholar]
45. Гаврилова AL, Qin CJ, Sommer RD, Rheingold AL, Bosnich B. J Am Chem Soc. 2002; 124:1714. [PubMed] [Google Scholar]
46. Chang CJ, Loh ZH, Shi C, Anson FC, Nocera DG. J Am Chem Soc. 2004;126:10013. [PubMed] [Google Scholar]
Chang CJ, Loh ZH, Shi C, Anson FC, Nocera DG. J Am Chem Soc. 2004;126:10013. [PubMed] [Google Scholar]
47. Kadish KM, Frémond L, Shen J, Chen P, Ohkubo K, Fukuzumi S, Ojaimi ME, Gros CP, Barbe J-M, Guilard R. Inorg Chem. 2009 г.;48:2571. [PubMed] [Google Scholar]
48. Бард А.Дж., Фолкнер Л.Р. Электрохимические методы: основы и приложения. 2. Джон Уайли и сыновья, инк.; Нью-Йорк: 2001. [Google Scholar]
49. Левич В.Г. Физико-химическая гидродинамика. Прентис-Холл, Инк; Englewood Cliffs, NJ: 1962. [Google Scholar]
50. Кутецкий Дж., Левич В.Г. Ж физ хим. 1958; 32:1565. [Google Scholar]
51. Ояма Н., Энсон ФК. Анальная хим. 1980;52:1192. [Google Scholar]
52. Kadish KM, Shen J, Frémond L, Chen P, Ojaimi ME, Chkounda M, Gros CP, Barbe J-M, Ohkubo K, Fukuzumi S, Guilard R. Inorg Chem. 2008;47:6726. [PubMed] [Академия Google]
53. Kadish KM, Frémond L, Ou Z, Shao J, Shi C, Anson FC, Burdet F, Gros CP, Barbe J-M, Guilard R. J Am Chem Soc. 2005;127:5625. [PubMed] [Google Scholar]
2005;127:5625. [PubMed] [Google Scholar]
54. Фергюсон-Миллер С., Бэбкок Г.Т. Chem Rev. 1996; 96:2889. [PubMed] [Google Scholar]
55. Перейра М.М., Сантана М., Тейшейра М. Biochim Biophys Acta. 2001;1505:185. [PubMed] [Google Scholar]
56. Ким Э., Чуфан Э.Э., Камарадж К., Карлин К.Д. Chem Rev. 2004; 104:1077. [PubMed] [Google Scholar]
57. Chufán EE, Puiu SC, Karlin KD. Acc Chem Res. 2007; 40:563. [PubMed] [Академия Google]
58. Chishiro T, Shimazaki Y, Tani F, Tachi Y, Naruta Y, Karasawa S, Hayami S, Maeda Y. Angew Chem Int Ed. 2003;42:2788. [PubMed] [Google Scholar]
59. Collman JP, Boulatov R, Sunderlan CJ, Fu L. Chem Rev. 2004;104:561. [PubMed] [Google Scholar]
60. Collman JP, Boulatov R, Sunderland CJ. В: Справочник по порфиринам. Кадиш М., Смит К.М., Гилард Р., редакторы. Том. 11. Академическая пресса; Сан-Диего, Калифорния: 2003. с. 1. [Google Scholar]
61. Collman JP, Ghosh S, Dey A, Decreau RA, Yang Y. J Am Chem Soc. 2009 г.;131:5034. [Бесплатная статья PMC] [PubMed] [Google Scholar]
2009 г.;131:5034. [Бесплатная статья PMC] [PubMed] [Google Scholar]
62. Anson FC, Shi A, Steiger B. Acc Chem Res. 1997; 30:437. [Google Scholar]
63. Kjaergaard CH, Rossmeisl J, Nørskov JK. Неорг хим. 2010;49:3567. [PubMed] [Google Scholar]
64. Халиме З., Котани Х., Фукузуми С., Карлин К.Д. Proc Natl Acad Sci USA. 2011;108:13990. [Бесплатная статья PMC] [PubMed] [Google Scholar]
65. Ghiladi RA, Huang HW, Moënne-Loccoz P, Stasser J, Blackburn NJ, Woods AS, Cotter RJ, Incarvito CD, Rheingold AL, Karlin KD. J Biol Inorg Chem. 2005;10:63. [PubMed] [Академия Google]
66. Шин Х., Ли Д.Х., Кан С., Карлин К.Д. Электрохим Акта. 2003;48:4077. [Google Scholar]
67. Messerschmidt A. Adv Inorg Chem. 1993;40:121. [Google Scholar]
68. Джоко К.Ю., Чонг Л.С., Уэдд А.Г., Сяо З. J Am Chem Soc. 2010;132:2005. [PubMed] [Google Scholar]
69. Kosman D. J Biol Inorg Chem. 2010;15:15. [PubMed] [Google Scholar]
70. Соломон Э.И., Гинсбах Дж. В., Хеппнер Д.Е., Кибер-Эммонс М.Т., Кьяргаард Ч., Смитс П.Дж., Тиан Л., Вуртинк Дж.С. Фарадей Обсудить. 2011;148:11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
В., Хеппнер Д.Е., Кибер-Эммонс М.Т., Кьяргаард Ч., Смитс П.Дж., Тиан Л., Вуртинк Дж.С. Фарадей Обсудить. 2011;148:11. [Бесплатная статья PMC] [PubMed] [Google Scholar]
71. Крэкнелл Дж.А., Винсент К.А., Армстронг Ф.А. Chem Rev. 2008; 108:2439. [PubMed] [Google Scholar]
72. Соломон Э.И., Сундарам Ю.М., Мачонкин Т.Е. Chem Rev. 1996; 96:2563. [PubMed] [Google Scholar]
73. Гевирт А.А., Торум М.С. Неорг хим. 2010;49:3557. [PubMed] [Google Scholar]
74. Fujieda N, Yakiyama A, Itoh S. Dalton Trans. 2010;39:3083. [PubMed] [Google Scholar]
75. Mirica LM, Ottenwaelder X, Stack TDP. Chem Rev. 2004; 104:1013. [PubMed] [Академия Google]
76. Льюис Э.А., Толман В.Б. Chem Rev. 2004; 104:1047. [PubMed] [Google Scholar]
77. Хэтчер Л.К., Карлин К.Д. J Biol Inorg Chem. 2004; 9:669. [PubMed] [Google Scholar]
78. Хэтчер Л.К., Карлин К.Д. Adv Inorg Chem. 2006; 58:131. [Google Scholar]
79. Фукузуми С., Котани Х., Лукас Х.Р., Дои К., Суэнобу Т. , Петерсон Р.Л., Карлин К.Д. J Am Chem Soc. 2010;132:6874. [Бесплатная статья PMC] [PubMed] [Google Scholar]
, Петерсон Р.Л., Карлин К.Д. J Am Chem Soc. 2010;132:6874. [Бесплатная статья PMC] [PubMed] [Google Scholar]
80. Tahsini L, Kotani H, Lee Y-M, Cho J, Nam W, Karlin KD, Fukuzumi S. Chem-Eur J. doi: 10.1002/chem.201103215. принято к публикации. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
81. Karlin KD, Haka MS, Cruse RW, Gultneh Y. J Am Chem Soc. 1985;107:5828. [Google Scholar]
82. Karlin KD, Tyeklár Z, Farooq A, Haka MS, Ghosh P, Cruse RW, Gultneh Y, Hayes JC, Toscano PJ, Zubieta J. Inorg Chem. 1992; 31:1436. [Google Scholar]
83. Пидкок Э., Обиас Х.В., Абэ М., Лян Х-К., Карлин К.Д., Соломон Э.И. J Am Chem Soc. 1999;121:1299. [Google Scholar]
84. Хенсон М.Дж., Мукерджи П., Рут Д.Э., Stack TDP, Соломон Э.И. J Am Chem Soc. 1999;121:10332. [Академия Google]
85. Que L, Jr, Tolman WB. Angew Chem Int Ed. 2002;41:1114. [PubMed] [Google Scholar]
86. Zhang J, Anson FC. Электрохим Акта. 1993;38:2423. [Google Scholar]
87. Lei Y, Anson FC. Неорг хим. 1994; 33:5003. [Google Scholar]
Lei Y, Anson FC. Неорг хим. 1994; 33:5003. [Google Scholar]
88. Marques ALB, Zhang J, Lever ABP, Pietro WJ. J Electroanal Chem. 1995; 392:43. [Google Scholar]
89. Losada J, del Peso I, Beyer L. Inorg Chim Acta. 2001; 321:107. [Google Scholar]
90. Dias VLN, Fernandes EN, da Silva LMS, Marques EP, Zhang J, Marques ALB. J Источники питания. 2005;142:10. [Академия Google]
91. Венг Ю.С., Фан Ф.Р., Бард А.Дж. J Am Chem Soc. 2005; 127:17576. [PubMed] [Google Scholar]
92. Wang M, Xu X, Gao J, Jia N, Cheng Y. Russ J Electrochem. 2006; 42:878. [Google Scholar]
93. Pichon C, Mialane P, Dolbecq A, Marrot J, Riviere E, Keita B, Nadjo L, Secheresse F. Inorg Chem. 2007;46:5292. [PubMed] [Google Scholar]
94. Thorum MS, Yadav J, Gewirth AA. Angew Chem Int Ed. 2009; 48:165. [PubMed] [Google Scholar]
95. McCrory CCL, Ottenwaelder X, Stack TDP, Chidsey CED. J Phys Chem A. 2007; 111:12641. [PubMed] [Академия Google]
96. McCrory CCL, Devadoss A, Ottenwaelder X, Lowe RD, Stack TDP, Chidsey CED. J Am Chem Soc. 2011;133:3696. [Бесплатная статья PMC] [PubMed] [Google Scholar]
J Am Chem Soc. 2011;133:3696. [Бесплатная статья PMC] [PubMed] [Google Scholar]
97. Thorseth MA, Letko CS, Rauchfuss TB, Gewirth AA. Неорг хим. 2011;50:6158. [PubMed] [Google Scholar]
98. Selmeczi K, Reglier M, Giorgi M, Speier G. Coord Chem Rev. 2003; 245:191–201. [Google Scholar]
99. Koval IA, Gamez P, Belle C, Selmeczi K, Reedijk J. Chem Soc Rev. 2006;35:814–840. [PubMed] [Академия Google]
100. Коваль И.А., Селмецци К., Белле С., Филуз С., Сен-Аман Э., Готье-Люно И., Шуйтема А.М., ван Влит М., Гамес П., Рубо О., Люкен М., Кребс Б., Лутц М., Спек А.Л. , Pierre J-L, Reedijk J. Chem-Eur J. 2006;12:6138–6150. [PubMed] [Google Scholar]
101. Kodera M, Kawata T, Kano K, Tachi Y, Itoh S, Kojo S. Bull Chem Soc Jpn. 2003; 76: 1957–1964. [Google Scholar] (e) Ackermann J, Meyer F, Kaifer E, Pritzkow H. Chem Eur J. 2002; 8: 247–258. [PubMed] [Академия Google]
102. Neves A, Rossi LM, Bortoluzzi AJ, Szpoganicz B, Wiezbicki C, Schwingel E, Haase W, Ostrovsky S.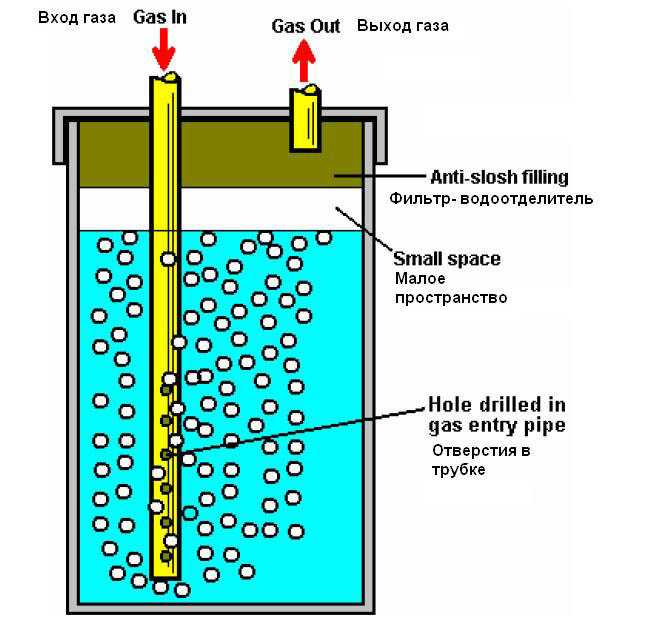 Inorg Chem. 2002; 41: 1788–1794. [PubMed] [Google Scholar]
Inorg Chem. 2002; 41: 1788–1794. [PubMed] [Google Scholar]
103. Балла Дж., Кисс Т., Джеймсон РФ. Неорг хим. 1992; 31: 58–62. [Google Scholar]
104. Chyn J-P, Urbach FL. Инорг Чим Акта. 1991; 189: 157–163. [Google Scholar]
105. Kaizer J, Csay T, Speier G, Giorgi M. J Mol Catal A-Chem. 2010; 329:71–76. [Google Scholar]
106. Kupán A, Kaizer J, Speier G, Giorgi M, Réglier M, Pollreisz F. J Inorg Biochem. 2009 г.;103:389–395. [PubMed] [Google Scholar]
107. Born K, Comba P, Daubinet A, Fuchs A, Wadepohl H. J Biol Inorg Chem. 2007; 12:36–48. [PubMed] [Google Scholar]
108. Брашетт Ф.Р., Торум М.С., Лиутас Н.С., Нотон М.С., Торноу С., Джонг Х.Р., Гевирт А.А., Кенис П.Я. J Am Chem Soc. 2010;132:12185. [PubMed] [Google Scholar]
109. Рамасами Р.П., Лукарифт Х.Р., Ивницкий Д.М., Атанасов П.Б., Джонсон Г.Р. хим. коммун. 2010;46:6045. [PubMed] [Google Scholar]
110. Wang Y, Zhou H. Chem Commun. 2010;46:6305. [PubMed] [Академия Google]
111. Yu H, Irie H, Hashimoto K. J Am Chem Soc. 2010;132:6898. [PubMed] [Google Scholar]
Yu H, Irie H, Hashimoto K. J Am Chem Soc. 2010;132:6898. [PubMed] [Google Scholar]
112. Wei W, Lu Y, Chen W, Chen S. J Am Chem Soc. 2011;133:2060. [PubMed] [Google Scholar]
113. Stephens IEL, Bondarenko AS, Perez-Alonso FJ, Calle-Vallejo F, Bech L, Johansson TP, Jepsen AK, Frydendal R, Knudsen BP, Rossmeisl J, Chorkendorff I. J Am хим. соц. 2011;133:5485. [PubMed] [Google Scholar]
114. Yi L, Song Y, Liu X, Wang X, Zou G, He P, Yi W. Int J Hydrogen Energy. 2011;36:15775. [Академия Google]
115. Cao D, Gao Y, Wang G, Miao R, Liu Y. Int J Hydrogen Energy. 2010;35:807. [Google Scholar]
116. Wu H, Wang C, Liu Z, Mao Z. Int J Hydrogen Energy. 2010;35:2648. [Google Scholar]
117. Charles JP, Russell RB, Yong KKRS. J Электрохим Soc. 2008;155:B558. [Google Scholar]
118. Hasvold O, Storkersen NJ, Forseth S, Lian T. J Power Sources. 2006; 162:935. [Google Scholar]
119. Yang W, Yang S, Sun W, Sun G, Xin Q. Electrochim Acta. 2006;52:9. [Google Scholar]
[Google Scholar]
120. Bewer T, Beckmann T, Dohle H, Mergel J, Stolten D. J Power Sources. 2004; 125:1. [Google Scholar]
121. Пратер Д.Н., Русек Дж.Дж. Приложение Энергия. 2003; 74:135. [Google Scholar]
122. Lao SJ, Qin HY, Ye LQ, Liu BH, Li ZP. J Источники питания. 2010;195:4135. [Google Scholar]
123. Тартаковский Б., Гио С.Р. Биотехнологическая прог. 2006; 22:241. [PubMed] [Google Scholar]
124. Jing X, Cao D, Liu Y, Wang G, Yin J, Wen Q, Gao Y. J Electroanal Chem. 2011;658:46. [Академия Google]
125. Ямазаки С., Сирома З., Сенох Х., Иорой Т., Фудзивара Н., Ясуда К. Дж. Источники питания. 2008;178:20. [Google Scholar]
126. Yamada Y, Yoshida S, Honda T, Fukuzumi S. Energy Environ Sci. 2011;4:2822. [Google Scholar]
127. Санли А.Е., Айтак А. Int J Hydrogen Energy. 2011;36:869. [Google Scholar]
128. Ruzgas T, Gorton L, Emnéus J, Marko-Varga G. J Electroanal Chem. 1995; 391:41. [Google Scholar]
129. Obinger C. Arch Biochem Biophys. 2010;500:1. [PubMed] [Академия Google]
Arch Biochem Biophys. 2010;500:1. [PubMed] [Академия Google]
130. Vidossich P, Alfonso-Prieto M, Carpena X, Fita I, Loewen PC, Rovira C. Arch Biochem Biophys. 2010;500:37. [PubMed] [Google Scholar]
131. Lin MJ, Fang X, Xu MB, Wang JD. Spectrochim ActaPart A. 2008; 71:1188. [PubMed] [Google Scholar]
Microsoft тестирует генераторы водорода — топливные элементы Microsoft
- Microsoft успешно использовала водород для резервного копирования части центра обработки данных в качестве доказательства концепции.
- Пока мы не сможем сделать производство водорода более рентабельным, мы получаем его, используя ископаемое топливо.
- Поскольку время безотказной работы намного превышает 99 процентов, реальный вариант использования этого резервного копирования — это крошечное количество времени.
В рамках своего плана по достижению нулевого уровня выбросов углерода к 2030 году Microsoft рассматривает возможность замены своих резервных дизельных генераторов водородными аккумуляторными батареями. Компания успешно поддерживала работу части одного из своих центров обработки данных в течение 48 часов только за счет водородной энергии.
Компания успешно поддерживала работу части одного из своих центров обработки данных в течение 48 часов только за счет водородной энергии.
Центры обработки данных — это огромные объекты, которые обычно заполнены серверами и любым другим компьютерным или телекоммуникационным оборудованием. В них могут храниться ежедневные или даже ежечасные резервные копии от финансовых учреждений и других пользователей с высоким спросом, потому что неправильная катастрофа может уничтожить всю внутреннюю сеть банка.
Погрузитесь глубже. Прочтите самые подробные статьи о науке и технике, разгадайте самые большие тайны жизни и получите неограниченный доступ ко всем вещам Pop Mech — , начиная с сегодняшнего дня.
Но центры обработки данных, а не только Microsoft, размещают большую часть Интернета без какого-либо фонаря резервного копирования или аварийного планирования. Это ваше облачное хранилище — там, например, размещен ваш веб-сайт Squarespace, и там хранятся миллиарды изображений продуктов Amazon.
Это ваше облачное хранилище — там, например, размещен ваш веб-сайт Squarespace, и там хранятся миллиарды изображений продуктов Amazon.
Резервное копирование центров обработки данных — это крошечная часть выбросов Microsoft, но, как и в большинстве центров обработки данных — и в большинстве случаев, и точка — дизельные генераторы являются просто отраслевым стандартом для резервного питания. Microsoft редко приходится использовать свои резервные генераторы, а на дизельное топливо приходится всего 1 процент выбросов Microsoft. Но это делает мощность центра обработки данных отличным тестовым примером для нового решения.
Связанная история
- Лучшие генераторы для дома
Оснащение центров обработки данных водородным резервным питанием — это большой проект, но он может создать дополнительную выгоду, чтобы помочь окупить себя. Из заявления Microsoft:
«ЦОД [Microsoft] Azure, оснащенный топливными элементами, резервуаром для хранения водорода и электролизером, который преобразует молекулы воды в водород и кислород, может быть интегрирован с электросетью для предоставления услуг балансировки нагрузки.Дальнемагистральные автомобили, работающие на водороде, могут [подъезжать] к центрам обработки данных, чтобы заполнить свои баки».
Последняя идея на удивление правдоподобна, поскольку центры обработки данных Microsoft разбросаны в некоторых центральных местах, по крайней мере, для транспорта континентальной части США. И первое предполагает, что Microsoft может попытаться имитировать то, что уже делают аккумуляторные фермы Tesla Илона Маска, сохраняя возобновляемую энергию, вырабатываемую ветром и солнцем. Хранение энергии в течение коротких периодов времени и подача ее обратно в сеть в периоды повышенного спроса, например, может снизить потребительские расходы и нагрузку на электростанции, работающие на ископаемом топливе.
История по теме
- Аккумуляторная ферма Илона Маска — бесспорный успех
Водород привлекателен для компаний, потому что это не сильно отличается от парадигмы ископаемого топлива, а поставщики ископаемого топлива в настоящее время являются основными поставщиками водорода, поэтому они рады пройти мантию.