- Процесс пиролиза — реакции, распад, факторы влияния, проблемы
- Пиролиз метана: понятие, реакция, уравнение, продукты
- Сети реакций пиролиза модельных соединений лигнина: распутывание термической деструкции соединений β-O-4 и α-O-4
- Механизмы реакций при пиролизе целлюлозы: обзор литературы (технический отчет)
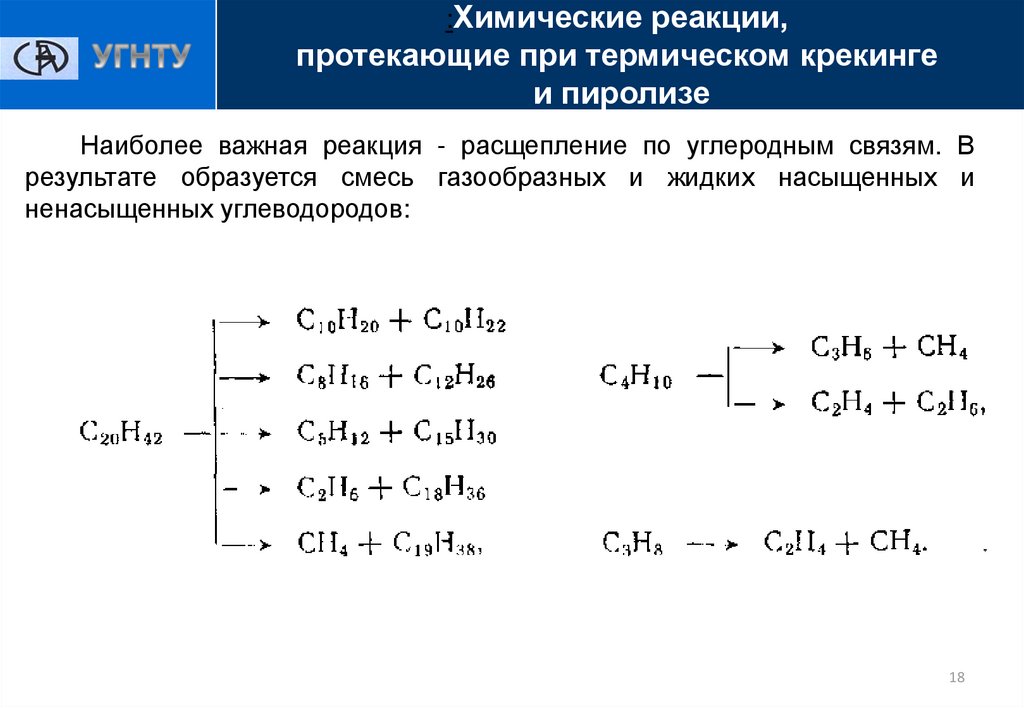
Процесс пиролиза — реакции, распад, факторы влияния, проблемы
Основными реакциями процесса пиролиза являются реакции разложения алканов и нафтеновых углеводородов на меньшие молекулы-осколки, которые, в свою очередь, вступают в разнообразные реакции между собой.
Предельные углеводороды
|
С12Н26—> |
С6Н14 |
+ С6Н12 |
|
додекан |
гексан |
Гексен |
С уменьшением молекулярного веса и ростом температуры распад молекулы происходит ближе к ее краю, при этом образуется легкий углеводород и тяжелый остаток молекулы, который быстро разлагается.
|
С6Н14 |
С2Н4 |
+ С4Н10 |
|
гексан |
этилен |
Бутан |
|
С4Н10 —> |
С2Н4 |
+ С2Н6 |
|
бутан |
этилен |
этан |
Распад изобутана при пиролизе протекает в основном в двух направлениях:
СН3 — СН — СН3 —> СН 2 = С — СН3 + Н2
¦ ¦
СН3 СН3
изобутан изобутилен
СН3 — СН — СН3 —> СН2 = СН — СН3 + СН4
¦ пропилен метан
СН3
изобутан
В этих реакциях этилен не образуется. Если основной задачей является получение максимального количества этилена, то изобутан считается нежелательным компонентом сырья пиролиза.
Если основной задачей является получение максимального количества этилена, то изобутан считается нежелательным компонентом сырья пиролиза.
При пиролизе этановой фракции реакция проходит по следующей схеме:
|
С2Н6 —> |
С2Н4 |
+ Н2 |
|
этан |
этилен |
водород |
При пиролизе рецикловых сбросов с высоким содержанием пропана реакция проходит по следующей схеме:
|
С3Н8 —> |
С2Н4 |
+ СН4 |
|
пропан |
этилен |
Метан |
|
С3Н8 —> |
С3Н6 |
+ Н2 |
|
пропан |
пропилен |
Водород |
Непредельные углеводороды
Непредельные углеводороды — олефины, являются конечным продуктом пиролиза, поэтому присутствие их в сырье нежелательно.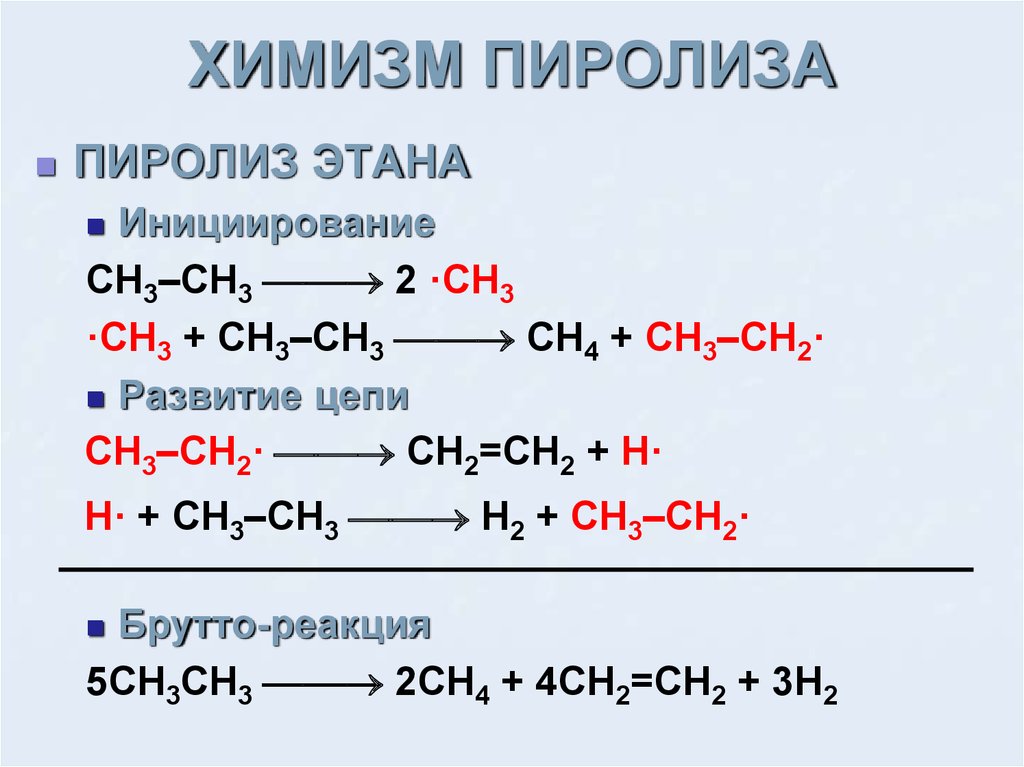 При температуре 600 оС и выше реакция распада олефинов сопровождается реакциями конденсации с образованием непредельных углеводородов с двумя двойными связями — диолефинов.
При температуре 600 оС и выше реакция распада олефинов сопровождается реакциями конденсации с образованием непредельных углеводородов с двумя двойными связями — диолефинов.
2СН2 = СН2 —> СН2 = СН — СН = СН2 + Н2
этиленбутадиен
При дальнейшей конденсации образуются ароматические углеводороды.
СН2 = СН — СН = СН2 + СН2 = СН2 —> С6Н6 + 2Н2
бутадиен этилен бензол
Устойчивость олефинов к действию высоких температур понижается с увеличением числа атомов углерода в молекуле. Этилен является наиболее устойчивым из непредельных углеводородов, но при температуре выше 650
|
4С2Н4 |
—> 2С4Н8 |
+ 4Н2 |
|
|
бутен |
|
При температуре выше 600 оС для этилена характерны реакция конденсации:
|
2С2Н4 |
—> С4Н6 |
+ Н2 |
|
|
бутадиен |
|
и присоединение водорода:
|
С2Н4 |
+ Н2—> |
С2Н6 |
|
|
|
этан |
Нафтеновые углеводороды
Нафтеновые углеводороды, например, циклопентан и циклогексан, более устойчивы к действию температуры, чем нормальные пентан и гексан.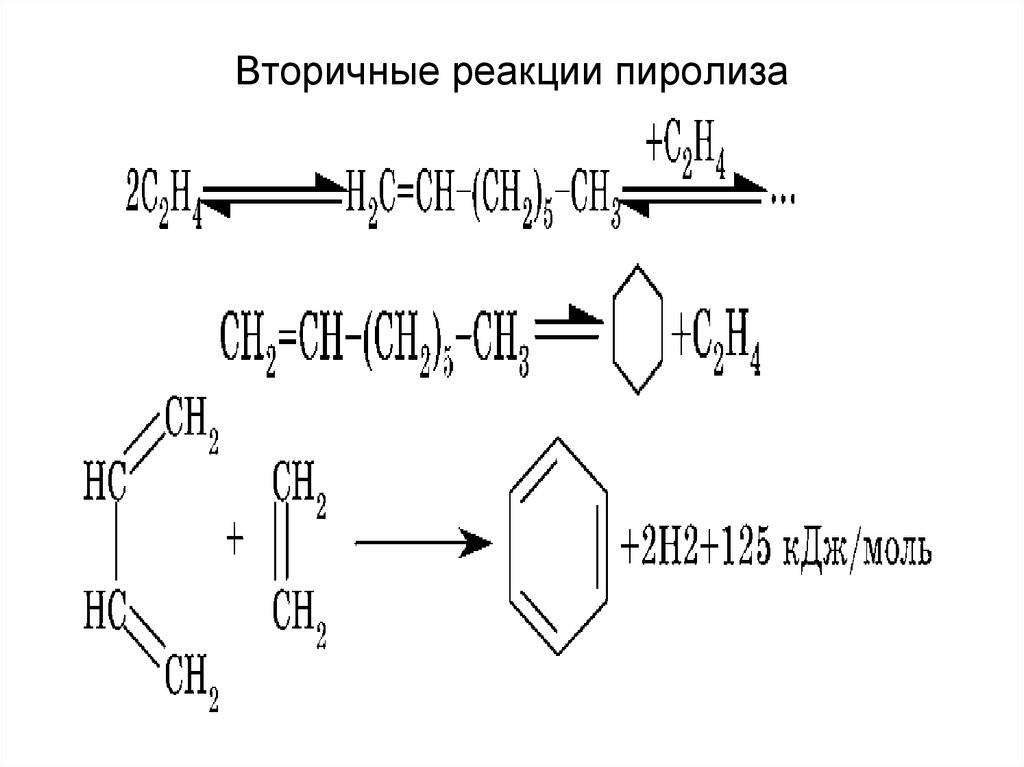
С увеличением длины боковой цепи устойчивость нафтеновых углеводородов понижается.
Сырье
Лучшим сырьем для процесса пиролиза являются предельные углеводороды. Их используют в смеси с другими углеводородами, которые также участвуют в процессе.
Температура
Температура является одним из основных факторов, определяющих процесс пиролиза. При повышении температуры резко повышается скорость реакции пиролиза, иногда меняется их характер.
С повышением температуры скорость первичных реакций распада растет быстрее, чем вторичных реакций полимеризации и конденсации. Поэтому непредельные углеводороды (этилен, пропилен) сохраняются в пирогазе и выход их на сырье возрастает, а выход смолы и кокса снижается.
Время контакта
Это время, в течение которого углеводороды находятся в зоне высоких температур (в реакционной зоне).
С увеличением времени контакта пирогаза в зоне высоких температур снижается выход этилена и пропилена, увеличивается коксообразование.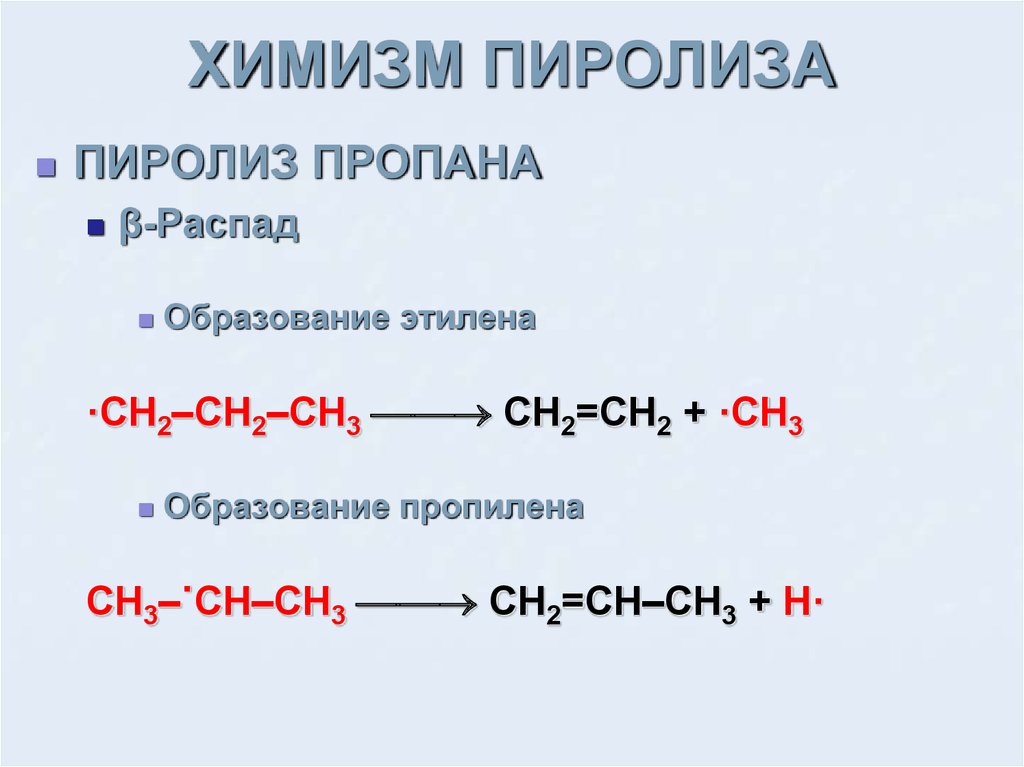
Давление
Снижение давления способствует образованию газообразных продуктов реакции, увеличению выхода этилена и пропилена. Увеличение давления приводит к увеличению выхода смол и кокса, снижению выхода этилена и пропилена.
Добавка инертных разбавителей
Разбавление сырья водяным паром способствует увеличению выхода этилена и пропилена, снижает выход кокса. Разбавляя реагирующие вещества, водяной пар тем самым уменьшает вероятность столкновения между собой молекул непредельных углеводородов и снижает реакции полимеризации и конденсации.
Примерно технологическая схема печи выглядит следующим образом:
В качестве основной проблемы процесса можно выделить невозможность наблюдения за происходящим с сырьем в реальном времени. Есть данные «что вошло», и данные о том «что получилось», однако любое воздействие на процесс возможно уже по факту свершившегося нарушения преобразований.
Пиролиз метана: понятие, реакция, уравнение, продукты
Какой станет наша планета через пару десятков лет – вот вопрос, который до сих пор мучает все человечество. Превратится ли наш дом в уютный уголок, или же постоянно расширяющаяся свалка скоро доберется до наших дворов? Переработка бытового мусора используется в развитых странах вот уже более 40 лет, но для России до сих пор являются чем-то новым. Тем более, что общественности практически ничего не известно о наиболее прогрессивных технологиях в сфере переработки мусора.
Превратится ли наш дом в уютный уголок, или же постоянно расширяющаяся свалка скоро доберется до наших дворов? Переработка бытового мусора используется в развитых странах вот уже более 40 лет, но для России до сих пор являются чем-то новым. Тем более, что общественности практически ничего не известно о наиболее прогрессивных технологиях в сфере переработки мусора.
Так, далеко не все из нас знают о том, что из обычного бытового мусора, которым забит каждый полигон ТБО, вернее из его органической составляющей при помощи такого устройства как биореактор можно получить биогаз – газ, имеющий в своем составе метан.
Полученная путем сжигания биогаза электроэнергия способна не только удовлетворить собственные нужды мусороперерабатывающего завода, но и использоваться для последующей продажи. Представьте себе, как это удобно, ведь из обычных отходов можно получить доходы. Причем данная технология переработки мусора является абсолютно безопасной и экологически чистой.
Однако полученный из мусора метан можно не только сжигать для получения тепла и электричества. Из метана путем процесса пиролиза можно получать ацителен. Что же это за вещество, и для чего оно нужно? Об этом мы поговорим чуть позже, а пока сделаем основной упор на самом процессе пиролиза метана.
Из метана путем процесса пиролиза можно получать ацителен. Что же это за вещество, и для чего оно нужно? Об этом мы поговорим чуть позже, а пока сделаем основной упор на самом процессе пиролиза метана.
Пиролиз метана реакция
Пиролиз метана это процесс, осуществляемый при высокой температуре в 1200-1500°С с последующим ему быстрым охлаждением продуктов реакции. В результате пиролиза образуется ацитилен, который здесь является скорее не конечной целью, а промежуточным продуктом, необходимым для дальнейшего производства продуктов органического синтеза. Поскольку пиролиз метана только для получения ацетилена экономически невыгоден, данная технология обычно применяется на заводах, осуществляющих его дальнейшую переработку в такие продукты как, например, синтетический каучук. Важным фактором, определяющим степень эффективности процесса пиролиза метана, является стойкость получаемых и исходных углеводородов при высокой температуре.
Судить о термической стойкости углеводородов можно по изменению в зависимости от температуры свободной энергии их образования. Чем ниже при данной температуре будет свободная энергия, тем стабильнее углеводород. Исследования данной зависимости показали, что стабильность ацетилена увеличивается с повышением температуры у, в то время как у других углеводородов стабильность падает. Это означает, что они при соответствующих условиях способны превратиться в ацетилен. Поскольку свободная энергия образования ацетилена при температуре 1200 °С меньше чем свободная энергия образования метана, то это сделало возможным образование ацетилена непосредственно из метана.
Чем ниже при данной температуре будет свободная энергия, тем стабильнее углеводород. Исследования данной зависимости показали, что стабильность ацетилена увеличивается с повышением температуры у, в то время как у других углеводородов стабильность падает. Это означает, что они при соответствующих условиях способны превратиться в ацетилен. Поскольку свободная энергия образования ацетилена при температуре 1200 °С меньше чем свободная энергия образования метана, то это сделало возможным образование ацетилена непосредственно из метана.
Однако ацетилен при 1500°С является термодинамически неустойчивым веществом, и в весьма короткий промежуток времени может разложиться на водород и углерод (сажу). Во избежание разложения получившегося в процессе пиролиза метана ацетилена время пребывания пиролизных газов в реакционной зоне ни в коем случае не должно превышать сотой доли секунды.
Продукты, полученные в результате реакции пиролиза метана, быстро охлаждаются до температуры 90—200 «С. Делается это для того, чтобы сохранить ацитилен, поскольку при такой температуре реакция разложения ацетилена прекращается. Охлаждение ацитилена производят путем впрыскивания в газовый поток воды. Данный процесс называется закалкой ацитилена.
Делается это для того, чтобы сохранить ацитилен, поскольку при такой температуре реакция разложения ацетилена прекращается. Охлаждение ацитилена производят путем впрыскивания в газовый поток воды. Данный процесс называется закалкой ацитилена.
Пиролиз метана уравнение
В настоящее время подробной кинетической схемы процесса пиролиза метана не существует. Однако метод и реакции пиролиза можно представить в виде ряда химических уравнений. Ацетилен добывают из метана путем термического разложения (пиролиза) по реакции:
2СН4 →С2Н2 + ЗН2 — 91 ккал
Для поддержания реакции пиролиза необходимо тепло, которое подводится путем нагрева исходных газов и образуется в результате сжигания непосредственно в реакционном объеме небольшого количества метана. В связи с тем фактом, что процесс пиролиза метана осуществляется в факеле, одновременно с образованием ацетилена протекает целый ряд побочных реакций, среди которых:
СН4 + 0,5О2 →СО + 2Н2 + 6,1 ккал
СН4 + 2О2 →СО2 + 2Н2О + 212 ккал
СО + Н2О →СО2 + Н2 + 10 ккал
С2Н2 →2С + Н2 + 18 ккал
Помимо указанных, также протекают и реакции образования высших ацетиленовых углеводородов, например, таких как диацетилен, метил ацетилен, винилацетилен и др.
Продукты пиролиза метана.
Ацетилен это бесцветный горючий газ с формулой C2H2. Данное вещество, которое по своей массе легче воздуха, обладает резким запахом. Ацетилен был впервые получен в 1836 году химиком Эдмондом Дэви, который получил его путем обработки карбида калия водой. Тогда ацетилен было решено использовать для освещения улиц. Ацетиленовые горелки давали примерно в 15 раз больше света, нежели обычные газовые фонари на метане, которыми освещали улицы. С течением времени они были вытеснены электрическими фонарями, но еще долго использовались в отдельных местностях.
Данное вещество так и осталось бы забытым, если бы не развитие химической промышленности не нашло ему новое применение. В середине прошлого века ацетилен нашел все более широкое применение в качестве исходного сырья при производстве самых различных химических продуктов. Ацитилен используется для получения:
- мономеров для хлоропренового каучука
- различных пластических масс (поливинилхлорид, поливинилацет)
- химических волокон
- растворителей
- Комментарии к статье
- Вконтакте
Сети реакций пиролиза модельных соединений лигнина: распутывание термической деструкции соединений β-O-4 и α-O-4
Сети реакций пиролиза для модельных соединений лигнина: распутывание термической деконструкции соединений β-O-4 и α-O-4†
Йонг С. Чой, и Рахул
Сингх, б Цзин
Чжан, и Ганеша
Баласубраманян, б Мэтью Р.
Осетр, c Руи
Катахира,
Чой, и Рахул
Сингх, б Цзин
Чжан, и Ганеша
Баласубраманян, б Мэтью Р.
Осетр, c Руи
Катахира,
Принадлежности автора
* Соответствующие авторы
и Кафедра химической и биологической инженерии, Университет штата Айова, Эймс, ИА 50011, США
Электронная почта: bshanks@iastate. edu
edu
б Факультет машиностроения, Университет штата Айова, Эймс, IA 50011, США
с Национальный центр биоэнергетики, Национальная лаборатория возобновляемых источников энергии, Голден, Колорадо 80401, США
Аннотация
Хотя лигнин является одним из основных компонентов биомассы, химия его пиролиза изучена недостаточно из-за сложной гетерогенности. Чтобы лучше понять эту химию, пиролиз семи модельных соединений лигнина (пять связанных молекул β-O-4 и две молекулы α-O-4) был исследован в микропиролизере, подключенном к ГХ-МС/ПИД. В соответствии с количественным молярным балансом продукта для реакционных сетей, согласованная фрагментация ретроена и гомолитическая диссоциация были настоятельно предложены в качестве начальной стадии реакции для соединений β-O-4 и соединений α-O-4 соответственно. Считалось, что разница в пути реакции между соединениями с разными связями является результатом термодинамики инициирования радикалов. Константы скорости для различных путей реакции были предсказаны из ab initio Расчеты теории функционала плотности и предэкспоненциальные литературные значения. Результаты расчетов согласуются с результатами эксперимента, что еще раз подтверждает различные механизмы пиролиза для соединений, связанных β-эфиром и α-эфиром. Комбинация двух путей из димерных модельных соединений позволила качественно описать пиролиз тримерного модельного соединения лигнина, содержащего связи как β-O-4, так и α-O-4.
Чтобы лучше понять эту химию, пиролиз семи модельных соединений лигнина (пять связанных молекул β-O-4 и две молекулы α-O-4) был исследован в микропиролизере, подключенном к ГХ-МС/ПИД. В соответствии с количественным молярным балансом продукта для реакционных сетей, согласованная фрагментация ретроена и гомолитическая диссоциация были настоятельно предложены в качестве начальной стадии реакции для соединений β-O-4 и соединений α-O-4 соответственно. Считалось, что разница в пути реакции между соединениями с разными связями является результатом термодинамики инициирования радикалов. Константы скорости для различных путей реакции были предсказаны из ab initio Расчеты теории функционала плотности и предэкспоненциальные литературные значения. Результаты расчетов согласуются с результатами эксперимента, что еще раз подтверждает различные механизмы пиролиза для соединений, связанных β-эфиром и α-эфиром. Комбинация двух путей из димерных модельных соединений позволила качественно описать пиролиз тримерного модельного соединения лигнина, содержащего связи как β-O-4, так и α-O-4.
Механизмы реакций при пиролизе целлюлозы: обзор литературы (технический отчет)
Механизмы реакций при пиролизе целлюлозы: обзор литературы (технический отчет) | ОСТИ.GOVперейти к основному содержанию
- Полная запись
- Другое связанное исследование
Представлен библиографический обзор из 195 источников, отражающий историю изучения механизмов пиролиза целлюлозы. Обсуждаемые темы: идентификация начального продукта, механизм начального образования левоглюкозана из целлюлозы и родственных соединений, разложение целлюлозы на другие соединения, образование ароматических соединений, пиролиз левоглюкозана, сшивание целлюлозы, пиролитические реакции производных целлюлозы и эффекты. неорганических солей на механизм пиролиза. (ДжСР)
неорганических солей на механизм пиролиза. (ДжСР)
- Авторов:
- Молтон, П. М.; Деммит, Т. Ф.
- Дата публикации:
- Исследовательская организация:
- Battelle Pacific Northwest Labs., Ричленд, Вашингтон (США)
- Идентификатор ОСТИ:
- 7298596
- Номер(а) отчета:
- БНВЛ-2297
- Номер контракта Министерства энергетики:
- EY-76-C-06-1830
- Тип ресурса:
- Технический отчет
- Страна публикации:
- США
- Язык:
- Английский
- Тема:
- 37 НЕОРГАНИЧЕСКАЯ, ОРГАНИЧЕСКАЯ, ФИЗИЧЕСКАЯ И АНАЛИТИЧЕСКАЯ ХИМИЯ; 09 ТОПЛИВО НА БИОМАССЕ; ЦЕЛЛЮЛОЗА; ПИРОЛИЗ; КИНЕТИКА ХИМИЧЕСКИХ РЕАКЦИЙ; ВЫХОД ХИМИЧЕСКОЙ РЕАКЦИИ; ОБЗОРЫ; УГЛЕВОДЫ; ХИМИЧЕСКИЕ РЕАКЦИИ; РАЗЛОЖЕНИЕ; ТИПЫ ДОКУМЕНТОВ; КИНЕТИКА; ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ; ПОЛИСАХАРИДЫ; КИНЕТИКА РЕАКЦИИ; САХАРИДЫ; ТЕРМОХИМИЧЕСКИЕ ПРОЦЕССЫ; УРОЖАЙНОСТЬ; 400800* — Горение, пиролиз и высокотемпературная химия; 090400 — Твердые отходы и древесное топливо- (-1989)
Форматы цитирования
- MLA
- АПА
- Чикаго
- БибТекс
Молтон П. М. и Деммитт Т.Ф. Механизмы реакций при пиролизе целлюлозы: обзор литературы . США: Н. П., 1977.
Веб. дои: 10.2172/7298596.
М. и Деммитт Т.Ф. Механизмы реакций при пиролизе целлюлозы: обзор литературы . США: Н. П., 1977.
Веб. дои: 10.2172/7298596.
Копировать в буфер обмена
Молтон П.М. и Деммитт Т.Ф. Механизмы реакций при пиролизе целлюлозы: обзор литературы . Соединенные Штаты. https://doi.org/10.2172/7298596
Копировать в буфер обмена
Молтон, П.М., и Деммитт, Т.Ф., 1977.
«Механизмы реакций при пиролизе целлюлозы: обзор литературы». Соединенные Штаты. https://doi.org/10.2172/7298596. https://www.osti.gov/servlets/purl/7298596.
Копировать в буфер обмена
@статья{osti_7298596,
title = {Механизмы реакций при пиролизе целлюлозы: обзор литературы},
автор = {Молтон П. М. и Деммитт Т.Ф.},
М. и Деммитт Т.Ф.},
abstractNote = {Представлен библиографический обзор 195 ссылок, отражающий историю изучения механизмов пиролиза целлюлозы. Обсуждаемые темы: идентификация начального продукта, механизм начального образования левоглюкозана из целлюлозы и родственных соединений, разложение целлюлозы на другие соединения, образование ароматических соединений, пиролиз левоглюкозана, сшивание целлюлозы, пиролитические реакции производных целлюлозы и эффекты. неорганических солей на механизм пиролиза. (JSR)},
дои = {10,2172/7298596},
URL = {https://www.osti.gov/biblio/7298596},
журнал = {},
номер =,
объем = ,
место = {США},
год = {1977},
месяц = {8}
}
Копировать в буфер обмена
Посмотреть технический отчет (2,86 МБ)
https://doi.org/10.2172/7298596
Экспорт метаданных
Сохранить в моей библиотеке
Вы должны войти в систему или создать учетную запись, чтобы сохранять документы в своей библиотеке.